- Libri preferiti
Accedi all'area personale per aggiungere e visualizzare i tuoi libri preferiti
Accedi all'area personale per aggiungere e visualizzare i tuoi libri preferiti
Pubblicazione: 1992
Tipo di risorsa: testo, Livello bibliografico: monografia, Lingua: , Paese:
Fa parte di: Enciclopedia medica italiana : aggiornamento della seconda edizione / editor Luciano Vella
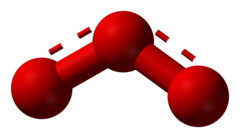
L'ozono (formula chimica: O3) è una forma allotropica dell'ossigeno, dal caratteristico odore agliaceo. Le sue molecole sono formate da tre atomi di ossigeno. Christian Friedrich Schönbein lo scoprì nel 1840, durante esperimenti di ossidazione lenta del fosforo bianco e di elettrolisi dell'acqua.

La riduzione dell'ozonosfera e il buco dell'ozonosfera sono due fenomeni connessi con la riduzione dell'ozono stratosferico, intendendosi con essi rispettivamente: il calo lento, relativamente stabile e globale dell'ozono stratosferico totale ovvero nell'ozonosfera dai primi anni '80 in poi; il molto più potente, ma intermittente fenomeno della riduzione dell'ozono delle regioni polari terrestri, quello a cui più propriamente ci si riferisce quando si parla di "buco dell'ozono", in realtà un assottigliamento marcato dello strato stesso.Lo strato di ozono è uno schermo fondamentale per l'intercettazione di radiazioni letali per la vita sulla Terra, e la sua formazione avviene principalmente nella stratosfera alle più irradiate latitudini tropicali, mentre la circolazione globale tende poi ad accumularlo maggiormente alle alte latitudini e ai poli. Il meccanismo di formazione del buco è diverso dall'assottigliamento alle medie latitudini dello strato di ozono, ma entrambi i fenomeni si basano sul fatto che gli alogeni, principalmente cloro e bromo, catalizzano reazioni ozono-distruttive. I composti responsabili appaiono essere principalmente dovuti all'azione umana. I fenomeni stratosferici non vanno confusi col fatto che l'ozono è un energico ossidante e per gli esseri viventi è un gas altamente velenoso, quindi dannoso se presente a bassa quota, dove può formarsi essendo uno dei contaminanti gassosi dell'inquinamento atmosferico, un inquinante secondario formantesi in seguito, in genere, a combustioni, con caratteristiche sterilizzanti verso ogni forma di vita. Invece, in alta quota, è un gas essenziale al mantenimento della vita sulla Terra, poiché assorbe le radiazioni dannose ultraviolette, e tale strato può assottigliarsi, ma non può del tutto scomparire, dato che, dopo lo strato di ozono, i raggi UV irraggerebbero l'ossigeno presente nello strato atmosferico successivo andando a ricreare ancora ozono.

L'ozonosfera è lo strato dell'atmosfera in cui si concentra la maggior parte dell'ozono, un gas serra "particolare": l'ozono trattiene e assorbe parte dell'energia proveniente direttamente dal Sole, in particolare le radiazioni a bassa lunghezza d'onda (o alta frequenza) nocive per la vita. L'ozono in oggetto si forma direttamente in stratosfera e non proviene dalla superficie terrestre come diversi altri gas serra. L'ozonosfera è stata scoperta nel 1913 dai fisici francesi Charles Fabry e Henri Buisson che notarono come la radiazione solare che raggiungeva la Terra fosse assimilabile con lo spettro di emissione di un corpo nero alla temperatura di 5.500–6.000 K (5.227-5.727°C) con la sola eccezione che vi fosse una lacuna nella zona dell'ultravioletto intorno ai 310 nm. Ne dedussero che la radiazione mancante fosse assorbita da qualcosa nell'atmosfera. Infine associarono la mancanza con il solo elemento chimico noto che potesse assorbire tale frequenza: l'ozono. Le caratteristiche dell'ozonosfera vennero poi studiate dal meteorologo britannico Gordon Dobson che costrui un apposito spettrometro (poi detto per l'appunto spettrometro di Dobson) che permetteva di misurare lo spessore dell'ozonosfera. Tra il 1928 e il 1958 Dobson diede vita a un rete mondiale di stazioni di monitoraggio dell'ozonosfera ancora attualmente operativa. In suo onore l'unità di misura convenzionalmente usata per indicare lo spessore della colonna di ozono si chiama Dobson.

L'ossigeno è un elemento chimico con numero atomico 8 (simbolo O). Fa parte degli elementi del gruppo 16 sulla tavola periodica ed è un agente non metallico altamente reattivo (ossidante) che forma facilmente ossidi e altri composti con la maggior parte degli elementi. Per massa, è il terzo elemento più abbondante dell'universo dopo l'idrogeno e l'elio. Il suo isotopo più stabile ha numero di massa 16. A temperatura e pressione standard due atomi dell'elemento si legano per formare una molecola di diossigeno (formula chimica O2), un gas incolore e inodore che costituisce il 20,8% dell'atmosfera terrestre (l'ossigeno è chimicamente troppo reattivo per rimanere un elemento libero nell'aria); legato ad altri elementi, è l'elemento chimico più comune della crosta terrestre, rappresentandone circa il 47% della massa, ed entra inoltre nella molecola dell'acqua. L'ossigeno è essenziale per la vita della maggior parte degli esseri viventi in quanto necessario alla respirazione; inoltre, le principali classi di molecole organiche presenti negli organismi viventi, come le proteine, gli acidi nucleici, i carboidrati e i lipidi, contengono ossigeno. Nelle attività umane viene comunemente utilizzato per l'ossigenoterapia, il sistema di supporto vitale degli aeromobili, dei sottomarini e dei veicoli spaziali, per le attività subacquee ricreative, come propellente per i razzi. Entra inoltre nei processi di produzione dell'acciaio e della plastica, nella brasatura, saldatura e il taglio di alcuni metalli, .
La classe dei composti organici volatili, (COV) o VOC (dall'inglese Volatile Organic Compounds), comprende diversi composti chimici le cui molecole contengono gruppi funzionali diversi: tali composti nel loro insieme hanno comportamenti fisici e chimici differenti, ma sono accomunati dal fatto che presentano un'elevata volatilità, caratteristica, ad esempio, dei comuni solventi organici aprotici apolari, come i diluenti per vernici e benzine. Tali composti comprendono gli idrocarburi liquidi in condizioni normali (contenenti, come elementi unici, carbonio e idrogeno, e che si dividono in alifatici e aromatici) e i composti contenenti ossigeno, cloro o altri elementi oltre al carbonio e l'idrogeno (detti "eteroatomi", come le aldeidi, gli eteri, gli alcooli, gli esteri, i clorofluorocarburi (CFC) e gli idroclorofluorocarburi (HCFC). La legislazione italiana definisce "composti organici volatili" quei composti organici che, alla temperatura di 293,15 K (20 °C), abbiano una pressione di vapore di 0,01 kPa o superiore.
Alcune catalogazioni sono state accorpate perché sembrano descrivere la stessa edizione. Per visualizzare i dettagli di ciascuna, clicca sul numero di record
Record aggiornato il: 2026-05-15T01:30:24.636Z